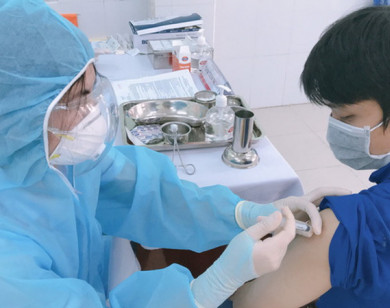
Tình nguyện viên đăng ký thử nghiệm lâm sàng vaccine Covid-19. Ảnh: baodantoc.vn
Theo Thông tư 11/2021/TT-BYT của Bộ Y tế ngày 19/8/2021 Hướng dẫn đăng ký lưu hành Vaccine phòng covid - 19 trong trường hợp cấp bách. Thông tư 11/2021/TT-BYT có hiệu lực từ ngày 19/8/2021 đến hết ngày 31/12/2022.
Trường hợp được miễn một, một số giai đoạn thử vaccine trên lâm sàng khi đăng ký lưu hành: Vaccine chưa đáp ứng quy định về dữ liệu lâm sàng để bảo đảm an toàn, hiệu quả trong hồ sơ đăng ký lưu hành vaccine thực hiện theo quy định tại điểm a, điểm b khoản 1 Điều 13 Thông tư số 32/2018/TT-BYT, được Bộ trưởng Bộ Y tế xem xét quyết định miễn một, một số giai đoạn thử thuốc trên lâm sàng (bao gồm cả miễn giảm dữ liệu lâm sàng) trên cơ sở ý kiến tư vấn của Hội đồng tư vấn cấp giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc khi thuộc một trong các trường hợp sau:
(1) Vaccine đã được cấp phép lưu hành tại ít nhất một nước trên thế giới và có dữ liệu lâm sàng về an toàn, hiệu quả.
Trường hợp cơ quan quản lý dược của nước đã cấp phép lưu hành không thuộc một trong các cơ quan quản lý quy định tại khoản 10 Điều 2 Thông tư số 32/2018/TT-BYT, sau khi được cấp giấy đăng ký lưu hành, cơ sở đăng ký phối hợp với cơ sở sản xuất phải tiếp tục đánh giá tính an toàn và tính sinh miễn dịch trên quần thể đích tại Việt Nam trong quá trình sử dụng theo hướng dẫn của Cục Khoa học công nghệ và Đào tạo - Bộ Y tế

Tuyển tình nguyện vên thử nghiệm lâm sàng vaccine ARCT-154 Việt nam. Ảnh: nld.com.vn
(2) Vaccine được sản xuất tại Việt Nam theo hình thức chuyển giao công nghệ một, một số hoặc toàn bộ các công đoạn của quy trình sản xuất thành phẩm mà trước chuyển giao công nghệ có dữ liệu lâm sàng về an toàn, hiệu quả đã được cấp phép lưu hành tại ít nhất một nước trên thế giới.
Trường hợp phải thử lâm sàng giai đoạn 4 tại Việt Nam: Trên cơ sở ý kiến tư vấn của Hội đồng tư vấn cấp giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc, vaccine đã được cấp giấy đăng ký lưu hành nhưng cần đánh giá thêm về an toàn, hiệu quả thì phải thử lâm sàng giai đoạn 4 tại Việt Nam.
Quy định về kiểm tra tính xác thực của các thông tin trên giấy tờ pháp lý, Thông tư này giao Cục Quản lý Dược phối hợp với các cơ quan ngoại giao và cơ quan có liên quan trong nước, nước ngoài, hoặc thông qua tra cứu thông tin tại trang thông tin điện tử trên hệ thống cơ sở dữ liệu tiếng Anh chính thức do cơ quan có thẩm quyền các nước cung cấp để thực hiện việc kiểm tra tính xác thực của Giấy chứng nhận sản phẩm dược phẩm (Certificate of Pharmaceutical Product (CPP), hoặc Giấy tờ pháp lý thay thế quy định tại điểm d khoản 2 Điều 15 Thông tư này của hồ sơ đề nghị cấp, gia hạn, thay đổi, bổ sung giấy đăng ký lưu hành vắc xin; Giấy tờ pháp lý do cơ quan quản lý nhà nước có thẩm quyền nước ngoài cấp đối với cơ sở đăng ký nước ngoài lần đầu đăng ký thuốc tại Việt Nam.

Học viện Quân y tiêm thử nghiệm lâm sàng vaccine Nano Covax Việt nam cho tình nguyện viên. Ảnh: thanhuytphcm.vn